医疗器械(UDI)唯一标识系统

![]()
苏州弘光条码提供UDI合规一站式服务:法规咨询、编码方案、赋码方案、产线贴码改造升级:
对于生产企业,您是否关心
◆ 什么是UDI?怎样解读政策?
◆ UDI的编码原则?UDI的载体?
◆ 如何赋码?数据、系统如何运作保障产品唯一性?
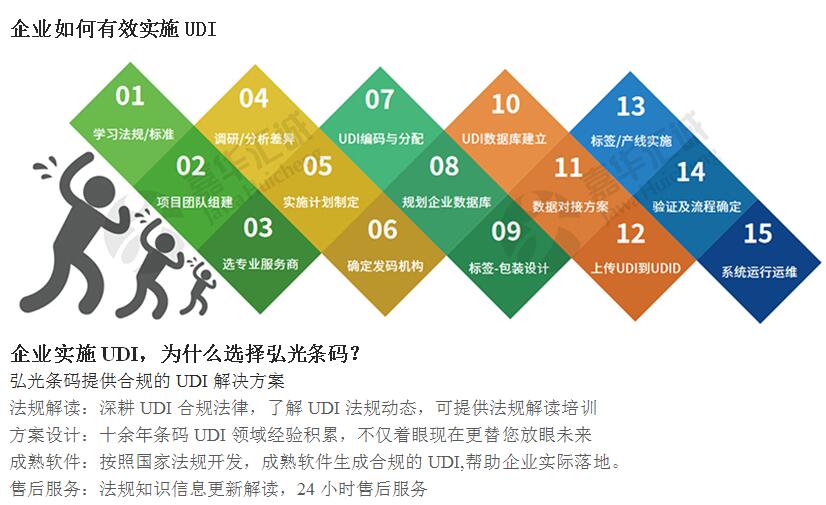
◆ UDI如何实施?找谁来实施?
◆ 产品什么时候需要UDI?如何统筹规划?
◆ 企业如何落地UDI,怎么申请DI,怎么生成UDI?
◆ U什么样的UDI是符合要求的?
◆ 我们都可以为你法规培训,企业生成落地,咨询电话:13584858298,汪经理
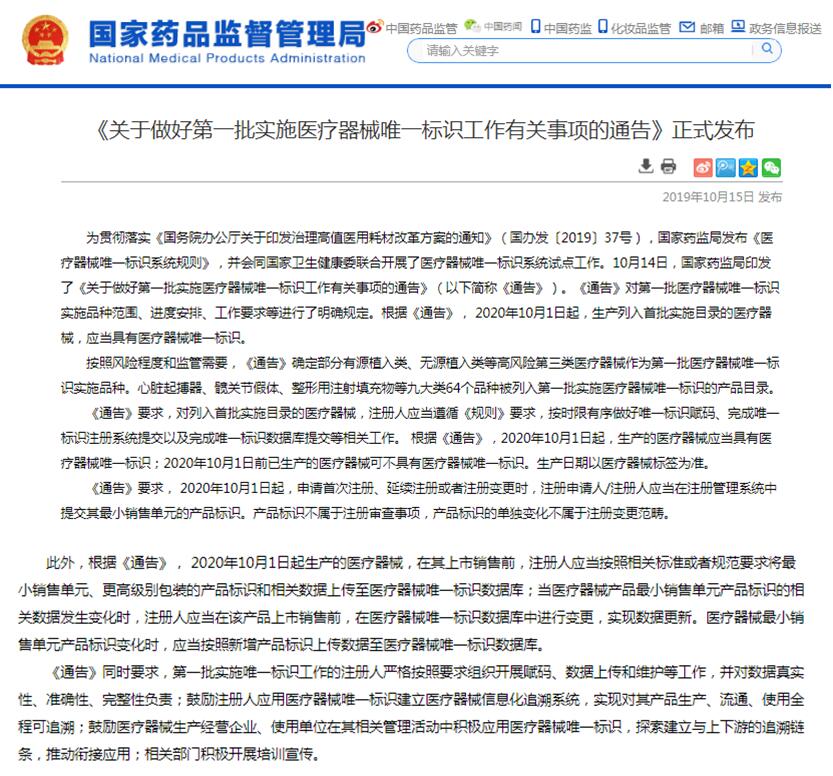
UDI实施的背景
国家药品监督管理局医疗器械法规管理要求内容如下
http://www.nmpa.gov.cn/WS04/CL2176/359233.html



![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()

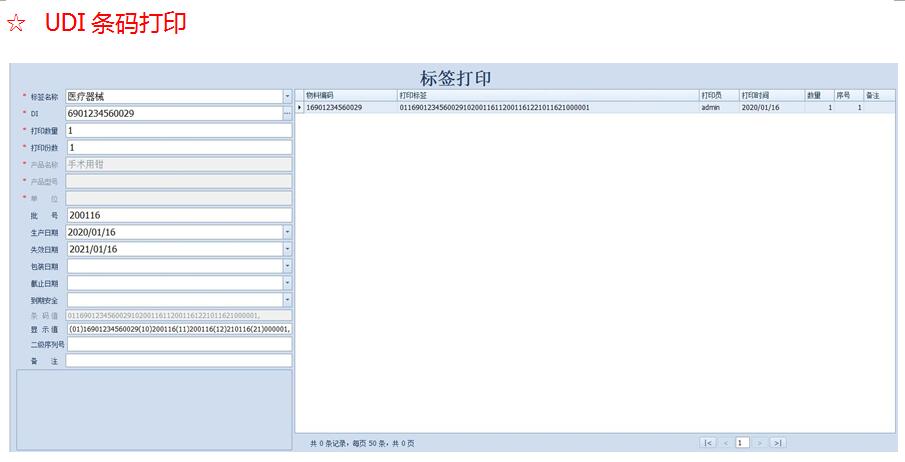
◆ 完整的国家级医疗器械唯一标识规则生成条码功能;
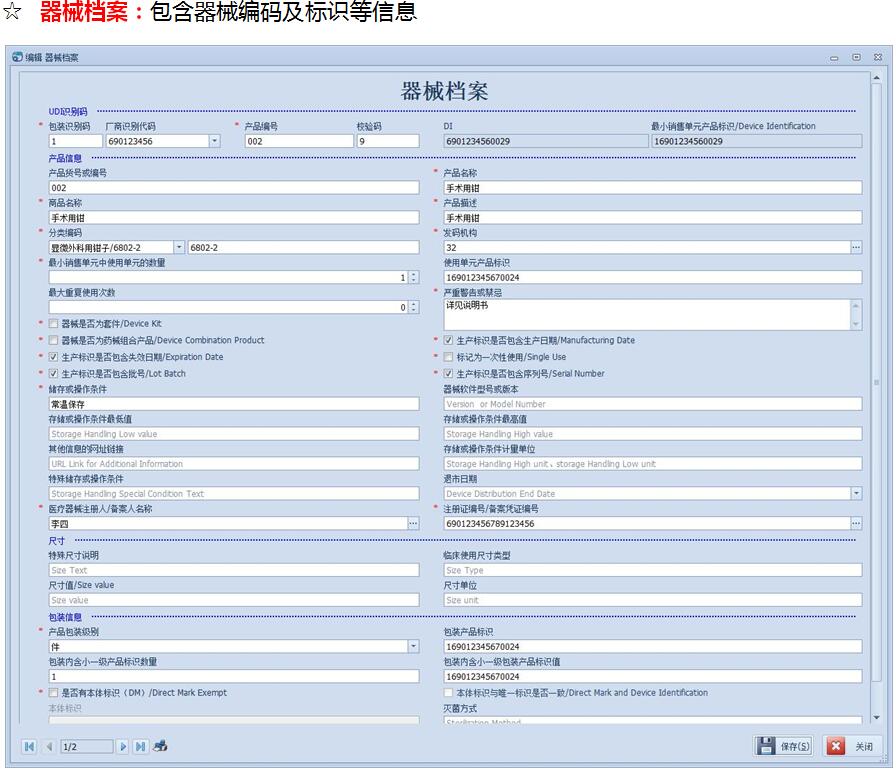
◆ 医疗器械唯一标识系统,由医疗器械唯一标识、唯一标识数据载体和唯一标识数据库组成;
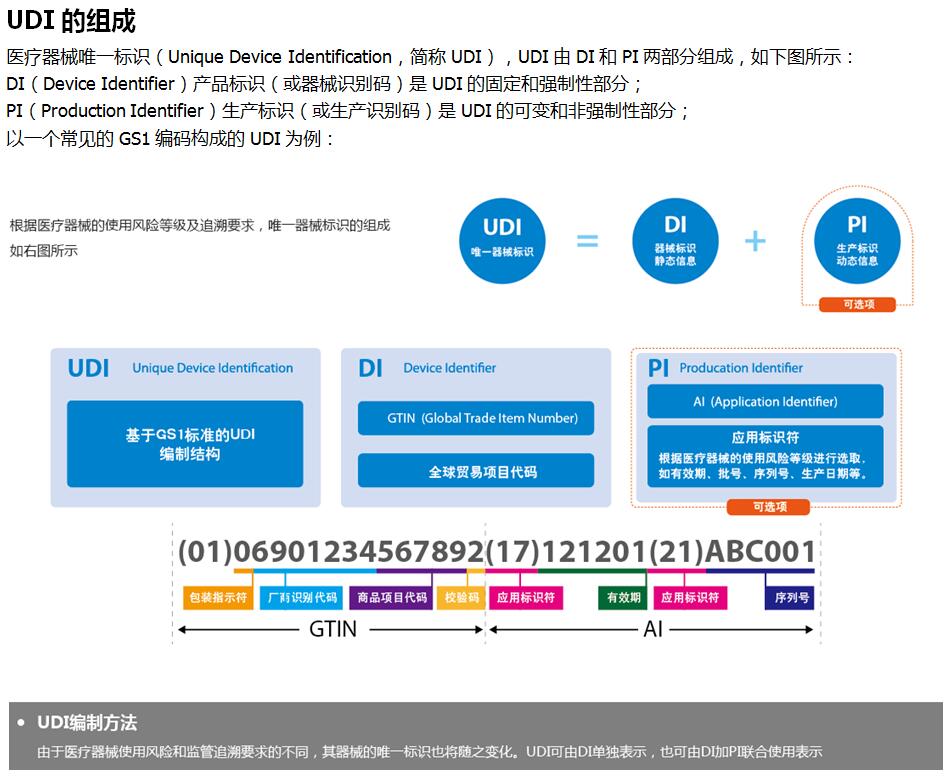
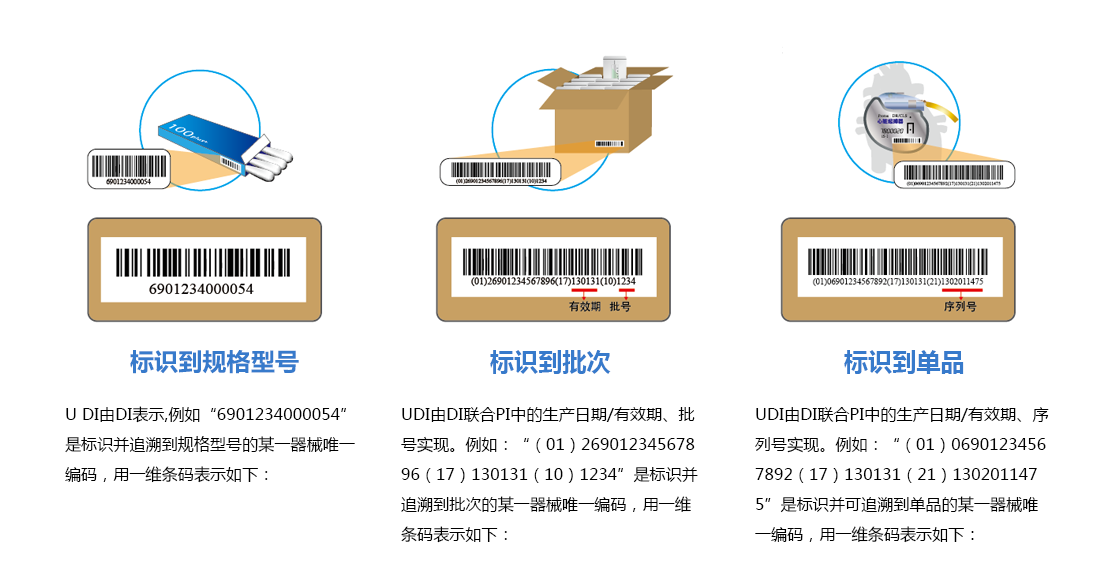
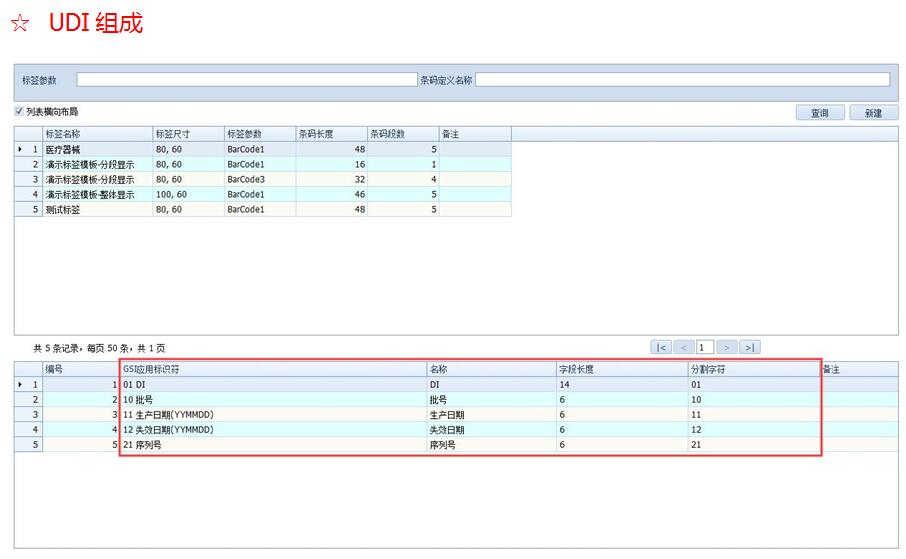
◆ UDI由两部分DI和PI组成;
◆ DI(Device Identifier):器械标识的静态信息,包含厂商识别代码和器械识别代码,该段信息需要上传国家数据库备案;
◆ PI(Production Identifier):生产识别的动态信息,包含生产日期、失效日期、批号、序列号等,贴标者可根据产品需要自主选择需要的信息,该段信息不需要上传;
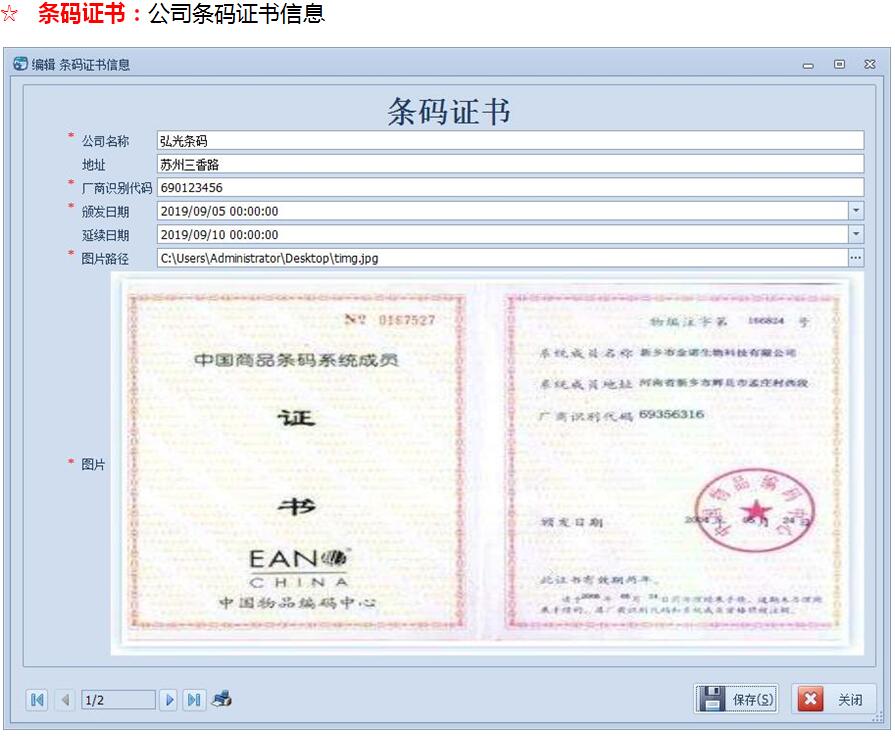
◆ 记录医疗器械的唯一标识数据库信息、注册人信息、发码机构信息、发码机构联系人信息、国内(一类、二类、三类)医疗器械信息、境外(一类、二类、三类)医疗器械信息、证照效期预警;